
HOSPITAL GENERAL PROVINCIAL DOCENTE
"DR ANTONIO LUACES IRAOLA"
CIEGO DE ÁVILA
Quilotórax neonatal
Neonatal chylothorax
Ana Iskra Meizoso ValdésI, Midiala Cervantes MederosI, Luis Alberto Rodríguez RodríguezII.
RESUMEN
Introducción:
el quilotórax congénito es una rara condición respiratoria,
sin embargo es la causa más frecuente de derrame pleural en
recién nacidos. Su incidencia es baja, aproximadamente 1:10 000-15 000
recién nacidos vivos. Las propuestas de tratamiento abarcan las
opciones conservadora, medicamentosa y quirúrgica.
Objetivo:
presentar el caso de un recién nacido con quilotórax
congénito tratado con suspensión de la alimentación oral y
administración parenteral de aminoácidos de cadena media y
ácidos grasos de cadena corta o media al reiniciar la
alimentación enteral.
Presentación del caso:
paciente masculino, primer gemelar pretérmino y bajo peso, con
síndrome parabiótico. A los 21 días de vida presentó
derrame pleural izquierdo. Se puncionó y el estudio del líquido
drenado mostró características propias del quilotórax. Se le
indicó tratamiento conservador, con alimentación parenteral
completa, y posteriormente con leche rica en ácidos grasos de cadenas
corta y media. Una vez recuperado se le dio el alta hospitalaria.
Conclusiones:
ante un neonato que presente signos clínicos y radiológicos de
derrame pleural se debe pensar en la posibilidad de un quilotórax, por
lo que es indispensable evacuar el líquido para su estudio. Una vez
confirmado el diagnóstico se sugiere la suspensión de la
alimentación por vía oral y administrar aminoácidos de
cadena media por vía parenteral. El reinicio de la alimentación
enteral debe ser con ácidos grasos de cadena corta o media, sin
ácidos grasos de cadena larga, para evitar las recidivas.
Palabras clave:
QUILOTÓRAX/epidemiología, QUILOTÓRAX/diagnóstico,
QUILOTÓRAX/tratamiento farmacológico, INFORMES DE CASOS.
ABSTRACT
Introduction:
congenital chylothorax is a rare respiratory condition, however it is the
most frequent cause of pleural effusion in newborns. Its incidence is low,
approximately 1:10 000-15 000 live births. Treatment proposals include
conservative, drug and surgical options.
Objective:
to present the case of a newborn with congenital chylothorax treated with
suspension of oral feeding and parenteral administration of medium chain
aminoacids and short or medium chain fatty acids upon reinitiation of
enteral feeding.
Case presentation:
male patient, first preterm twins and low weight, with parabiotic syndrome.
At 21 days of life he presented left pleural effusion. It was punctured and
the study of drained fluid showed characteristics of chylothorax.
Conservative treatment was indicated, with complete parenteral feeding, and
later with milk rich in fatty acids of short and medium chains. Once
recovered, he was discharged from hospital.
Conclusions:
in the presence of a neonate presenting clinical and radiological signs of
pleural effusion, the possibility of a chylothorax should be considered, so
it is essential to evacuate the fluid for study. Once the diagnosis is
confirmed, it is suggested to suspend the oral feeding and administer
medium chain amino acids parenterally. The restart of enteral feeding
should be with short or medium chain fatty acids, without long-chain fatty
acids, to avoid recurrence.
Keywords:
CHYLOTHORAX/epidemiology, CHYLOTHORAX/diagnosis, CHYLOTHORAX/drug therapy,
CASE REPORTS.
INTRODUCCIÓN
El quilotórax congénito (QC) es una rara condición
respiratoria, sin embargo es la causa más frecuente de derrame pleural
en recién nacidos (RN) vivos (65 %).(1-5) El derrame
pleural fetal o hidrotórax fetal se define como la presencia de
líquido en la cavidad torácica. Habitualmente se trata de un
hallazgo inespecífico que puede ser la manifestación de una serie
de afecciones subyacentes. Si el fluido contiene más de 1,1mm/L de
triglicéridos, la proporción de linfocitos es mayor de 80 % o su
aspecto macroscópico es lechoso, se trata de un quilotórax.
Habitualmente, el QC aparece secundario a una enfermedad linfática
generalizada, obstrucción venosa, compresión local del conducto
torácico o trauma obstétrico. Su incidencia es baja,
aproximadamente 1:10 000-15 000 RN vivos.(6)
Hasta la década de los '80 el QC se consideró un hallazgo radiológico en neonatos con dificultad respiratoria. Actualmente, mediante la ecografía Doppler, es posible diagnosticarlo en la etapa prenatal y descartar la hipótesis del traumatismo obstétrico como causa.(6-8) En 50 % de los casos, el QC se presenta en el momento del nacimiento o durante la primera semana de vida. Se asocia a diversos síndromes conocidos (síndromes de Turner, Noonan o Down) y a afecciones raras como la angiomatosis linfática sistémica, caracterizada por linfangiectasias (dilatación anterógrada de los conductos linfáticos), síndrome de Gorlin, trisomía 12q y síndrome de Opitz.(6)
En los neonatos el QC puede ser asintomático, pero durante la lactancia se acumula linfa en el espacio pleural o las extremidades. El cuadro clínico se caracteriza por la presencia de un síndrome de dificultad respiratoria, de gravedad variable en dependencia de la cuantía del derrame.(3,9-11) Su curso puede ser tórpido y son frecuentes las complicaciones (hipovolemia diselectrolitemias, hipoalbuminemia, hipogammaglobulinemia, hipofibrinogenemia) debidas a la pérdida de quilo y a la necesidad de tratamientos invasivos (drenaje torácico, ventilación mecánica y nutrición parenteral).(12) Las propuestas de tratamiento abarcan las opciones conservadora como la modificación dietética (nutrición parenteral total o dieta con triglicéridos de cadena media), medicamentosa (administración de octreótide o somatostatina) y quirúrgica.(11,12)
En la provincia de Ciego de Ávila no se habían reportado hasta el momento casos similares a este.
El objetivo de este trabajo es presentar un caso de quilotórax neonatal, de interés para los especialistas debido a lo poco frecuente de esta dolencia, la gravedad de sus complicaciones, la inexistencia de reportes de casos similares en el territorio, y su tratamiento basado en suspensión de la alimentación oral y administración parenteral de aminoácidos de cadena media y ácidos grasos de cadena corta o media al reiniciar la alimentación enteral.
PRESENTACIÓN DEL CASO
Paciente masculino, primer gemelar monocorial-monoamniótico
pretérmino, nacido por cesárea a las 27 semanas de gestación
con un peso de 1 170 g y Apgar 3/5. El segundo gemelar falleció a los
pocos minutos de vida producto de un síndrome parabiótico entre
gemelos, del que el primero fue el receptor.
Una vez en la sala el neonato fue acoplado al ventilador en modalidad controlada con altos parámetros. Durante el estudio, en la radiografía de tórax se observó enfermedad de la membrana hialina (EMH) grado IV, y se trató con tres dosis de surfactante exógeno. Dada la magnitud de la membrana, que es indistinguible de la neumonía de inicio precoz, también se le aplicó antimicrobiano. Fue transfundido debido a la anemia provocada por el síndrome parabiótico que presentó al nacer.
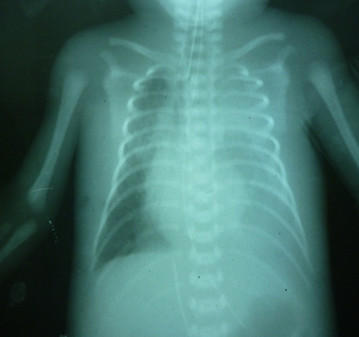
El paciente pasó por una fase de insuficiencia renal acompañada de edemas generalizados y oligoanuria y recibió tratamiento. Una vez recuperado se inició la disminución de los parámetros ventilatorios y se le instauró alimentación enteral y parenteral. A los 21 días de vida en la radiografía se observó una disminución de la transparencia del hemitórax izquierdo (figura 1) interpretada como un derrame pleural, diagnóstico confirmado por ultrasonido (figura 2).

Figura 1. Existe una disminución de la transparencia del hemitórax izquierdo compatible con derrame pleural.
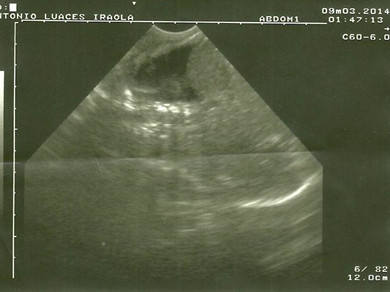
Figura 2. Imagen ultrasonográfica del derrame pleural.
Se puncionó el hidrotórax y se extrajeron 35 ml de líquido de aspecto lechoso, consistente con un quilotórax (figura 3).
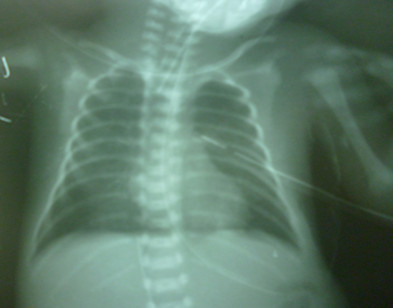
Figura 3. Imagen radiográfica después de la evacuación del quilotórax.
En el estudio citoquímico se comprobó que el líquido drenado tenía aspecto lechoso, color amarillo y contenido de glucosa de 6,6 mmol/L. La prueba de Rivalta mostró exudado y proteínas en 58,4 g/L, lactodesidrogenasa en 96, colesterol en 3,27, células en 347,6 y linfocitos al 100 %. En ese momento no se suspendió la alimentación enteral. La evolución posterior fue buena, y se pudo disminuir los parámetros ventilatorios hasta la modalidad espontánea.
Transcurridos siete días el neonato presentó la misma sintomatología y opacidad del pulmón izquierdo. El diagnóstico fue quilotórax recidivante. Se le realizó punción, se dejó pleurotomía con aspiración a pared y se suspendió la alimentación por vía oral. En las primeras 24 horas se aspiraron 90 ml de linfa, cantidad que disminuyó en los días posteriores hasta ser nulo el drenaje y se pinzó la pleurotomía para retirarla al día siguiente. Se reinició la alimentación oral con leche rica en ácidos grasos de cadena media y corta y nula en ácidos grasos de cadena larga (Portagen® de la firma Nestlé), tolerada sin dificultad (de acuerdo a la tolerancia y evolución del paciente se incrementó hasta alcanzar 16 ml cada tres horas).
Ocho días después de retirado el pleurótomo aparecieron edemas en el miembro inferior izquierdo, que luego se extendieron al tronco, cuello y cuero cabelludo. Posteriormente manifestó dificultad respiratoria e hiposaturación transcutánea con necesidad de incrementar los parámetros respiratorios. La radiografía de tórax mostró disminución de la transparencia en el hemitórax izquierdo y se constató por ultrasonido la presencia de líquido en la cavidad pleural bilateral, en mayor cuantía del lado izquierdo. Se puncionó ese lado y se drenaron 60 ml de contenido linfático. Se suspendió nuevamente la alimentación enteral y se mantuvo la alimentación parenteral con traximin y Lipofundin® al 10 %. El drenaje de linfa disminuyó hasta hacerse nulo y los edemas desaparecieron, por lo que se retiró el drenaje.
A los 70 días de ventilación el paciente fue extubado y se pasó a una modalidad de ventilación no invasiva (VNI) hasta llegar a respirar espontáneamente sin necesidad de apoyo. Posteriormente continuó la evolución hasta la recuperación con alimentación enteral con Neocate®, un tipo de leche rica en ácidos grasos de cadenas media y corta. Se le dio el alta a los tres meses de vida, con 2 500 g de peso. El neonato es evaluado periódicamente en la Consulta de Neurodesarrollo del servicio, donde se comprueba que mantiene buen estado de salud y un desarrollo psicomotor acorde a su edad.
DISCUSIÓN
El inicio precoz de la EMH puede estar relacionado al no uso en la madre de
inductores de la madurez pulmonar y la prematuridad extrema de estos
recién nacidos. Por su parte, los neonatos con QC pueden presentar
complicaciones propias de la afección y del tratamiento invasivo,
mortales en algunos casos. La presentación clínica es muy
variada, y se obstaculiza el diagnóstico, pero la dificultad
respiratoria de intensidad variable es parte esencial del cuadro
clínico. El estudio de las características del líquido
pleural permite confirmar el diagnóstico.(3,5)
En este caso no fue posible precisar la causa de su condición médica porque los procedimientos para llegar a un diagnóstico más preciso eran muy invasivos para el estado extremadamente crítico del neonato. El equipo quirúrgico optó por el tratamiento conservador y la observación de la evolución del paciente ya que, en ocasiones, pueden producirse pequeñas laceraciones u obstrucciones del conducto torácico que se resuelven espontáneamente, como pudo suceder en este caso.
Por otra parte, en la literatura revisada no se encontró asociación entre el síndrome parabiótico y el quilotórax neonatal, lo que tampoco se recoge en la etiología de esta afección.(5) El neonato respondió al tratamiento conservador con modificación dietética y no requirió tratamiento farmacológico con somatostatina (octreótide) ni quirúrgico.
CONCLUSIONES
Ante un neonato que presente signos clínicos y radiológicos de
derrame pleural se debe pensar en la posibilidad de un quilotórax, por
lo que es indispensable evacuar el líquido para su estudio. Una vez
confirmado el diagnóstico se sugiere la suspensión de la
alimentación por vía oral y administrar aminoácidos de
cadena media por vía parenteral. El reinicio de la alimentación
enteral debe ser con ácidos grasos de cadena corta o media, sin
ácidos grasos de cadena larga, para evitar las recidivas.
Conflictos de intereses
Los autores declaran que no existen conflictos de intereses.
REFERENCIAS BIBLIOGRÁFICAS
Recibido: 24 de abril de 2017
Aprobado: 1 de junio de 2017
| MsC. Ana Iskra Meizoso Valdés Hospital General Provincial Docente "Dr. Antonio Luaces Iraola" Calle Máximo Gómez No.257, entre 4ta y Onelio Hernández. Ciego de Ávila, Cuba. CP.65200 Correo electrónico: luisalberto@ali.cav.sld.cu |