
HOSPITAL GENERAL PROVINCIAL DOCENTE
"DR. ANTONIO LUACES IRAOLA"
CIEGO DE ÁVILA
Células madre. Generalidades (Parte II)
Stem cells. Generalities (Part II)
José Antonio Camacho AssefI, Lilian Camacho EscalanteII, Noslen Gómez MantillaIII, Volfredo Camacho AssefIV, Keidi López BorrotoV, Liliana García GonzálezVI.
RESUMEN
Introducción:
en Cuba la recolección de células madre autólogas se
realizaba mediante punción de las crestas ilíacas. Para ello se
requería anestesiar al paciente y disponer de un quirófano con el
personal capacitado y entrenado en la técnica. La introducción de
un método simplificado permitió extender el proceso a todas las
provincias del país.
Objetivo:
analizar información actualizada sobre el proceso de movilización
y el método manual para la recolección y procesamiento de las
células mononucleares de la médula ósea.
Método:
se revisó la literatura nacional e internacional sobre el tema en los
últimos 12 años, en español e inglés y en formatos
impreso y digital. La búsqueda en Internet abarcó varias bases de
datos y el buscador Google Académico. A partir de los materiales
seleccionados se elaboró una reseña estructurada.
Desarrollo:
las diferentes modalidades de trasplante de células madre
hematopoyéticas surgieron como alternativa terapéutica ante los
efectos adversos de las altas dosis de quimioterapia y radioterapia en
pacientes oncológicos. Sin embargo, mediante el trasplante
autólogo de células madre hematopoyéticas es posible
administrar al paciente dosis farmacológicas intensas con una
toxicidad hematopoyética y orgánica tolerable.
Conclusiones:
los conocimientos actuales sobre el proceso de movilización celular, y
el método manual para la recolección y procesamiento de las
células mononucleares de la médula ósea, abren posibilidades
alentadoras en la investigación básica y clínica. Las
propiedades exclusivas de estas células y la sencillez de su
procesamiento posibilitan su utilización en el tratamiento de
diferentes enfermedades.
Palabras clave:
CÉLULAS MADRE, CÉLULAS MADRE DE SANGRE PERIFÉRICA,
CÉLULAS MADRE HEMATOPOYÉTICAS, MOVILIZACIÓN DE CÉLULA
MADRE HEMATOPOYÉTICA/métodos, MOVILIZACIÓN, FACTOR
ESTIMULANTE DE COLONIAS DE GRANULOCITOS/uso terapéutico, TRASPLANTE
AUTÓLOGO, TRASPLANTE HOMÓLOGO, LITERATURA DE REVISIÓN COMO
ASUNTO.
ABSTRACT
Introduction:
in Cuba the collection of autologous stem cells was performed by puncture
of the iliac crests. To do this, it was necessary to anesthetize the
patient and have an operating room with qualified personnel trained in the
technique. The introduction of a simplified method allowed extending the
process to all the provinces of the country.
Objective:
to analize updated information about the mobilization process and the
manual method for the collection and processing of the bone marrow
mononuclear cells.
Method:
the national and international literature on the subject was reviewed in
the last 12 years, in Spanish and English, and in printed and digital
formats. The search on the Internet covered several databases and the
Google Scholar search engine. A structured review was prepared from the
selected materials.
Development:
the different modalities of hematopoietic stem cell transplantation emerged
as a therapeutic alternative to the adverse effects of high doses of
chemotherapy and radiotherapy in cancer patients. However, through
autologous hematopoietic stem cell transplantation, it is possible to
administer intense pharmacological doses to the patient with tolerable
hematopoietic and organic toxicity.
Conclusions:
the knowledge of the processes of self-renewal and differentiation of the
stem cells, the methods to mobilize them to the peripheral blood, collect
them and process them for their therapeutic use, opens up encouraging
possibilities in basic and clinical research. The exclusive properties of
these cells make possible their use in the treatment of different diseases.
Keywords:
STEM CELLS, PERIPHERAL BLOOD STEM CELLS, HEMATOPOIETIC STEM CELLS,
HEMATOPOIETIC STEM CELL MOBILIZATION/methods, GRANULOCYTE
COLONY-STIMULATING FACTOR/therapeutic use, AUTOLOGOUS TRANSPLANTATION,
HOMOLOGOUS TRANSPLANTATION, REVIEW LITERATURE AS TOPIC.
INTRODUCCIÓN
En Cuba, hace poco más de una década, la recolección de
células madre (CM) autólogas se realizaba mediante punción
de las crestas ilíacas. Para efectuar este procedimiento se
requería anestesiar al paciente y disponer de un quirófano con el
personal capacitado y entrenado en la técnica. La introducción de
un método simplificado permitió extender el proceso a todas las
provincias del país.
El objetivo de la presente revisión bibliográfica es recopilar información actualizada sobre el proceso de movilización y el método manual para la recolección y procesamiento de las células mononucleares de la médula ósea.
MÉTODO
Se revisó la literatura nacional e internacional sobre el tema,
publicada básicamente durante los últimos 12 años, en
español e inglés y en formatos impreso y digital. La
búsqueda en Internet abarcó la Biblioteca Virtual de Salud de
Cuba, las bases de datos Medline, EBSCO, PUBMED CUMED y LILACS y el
buscador Google Académico. Como criterios de búsqueda se
emplearon "células madre", "movilización", "factor estimulador de
colonias de granulocitos", "trasplante autólogo" y trasplante
alogénico. A partir de los materiales seleccionados se elaboró
una reseña estructurada.
DESARROLLO
Antecedentes del trasplante de progenitores hematopoyéticos
Las diferentes modalidades de trasplante de células madre
hematopoyéticas (CMH) surgieron como alternativa terapéutica ante
los efectos adversos de las altas dosis de quimioterapia y radioterapia en
pacientes oncológicos. Las dosis elevadas e intensificadas de estas
terapias causan toxicidad en diferentes órganos (médula
ósea, corazón, pulmones). Sin embargo, mediante el trasplante
autólogo de CMH es posible administrar al paciente dosis
farmacológicas intensas con una toxicidad hematopoyética y
orgánica tolerable.(1)
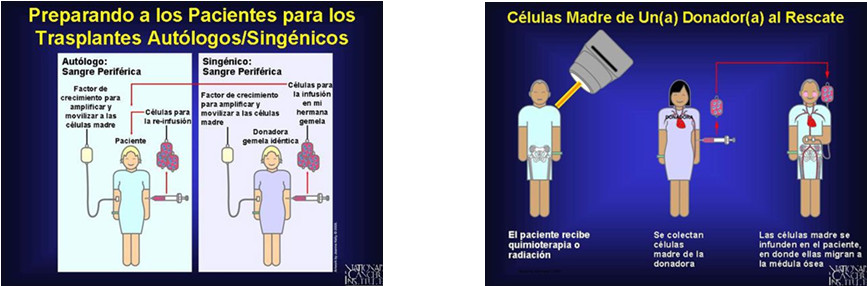
La expresión trasplante autólogo de CMH se utiliza a menudo de manera intercambiable con las expresiones trasplante autólogo de médula ósea (TaMO), trasplante autólogo de células madre de sangre periférica (TaCMSP) y trasplante autólogo de células hematopoyéticas (TACH). "Autólogo" significa que las células donantes utilizadas en el procedimiento se obtienen del propio paciente. En el caso del alotrasplante, el donante celular es distinto del paciente.(1) Una variante del alotrasplante, conocida como trasplante singénico, se realiza a partir de un donante gemelo idéntico del paciente (figura 1). En estos procedimientos alogénicos se emplea como fuente de CMH la sangre proveniente del cordón umbilical y la placenta (con posterioridad al parto).(2)

Figura 1. Tipos de trasplante hematopoyéticos
Fuente: https://www.pinterest.es/pin/506584658056831629/
Los resultados de los trasplantes de CMH evidenciaron que en la médula ósea (MO) existe un grupo heterogéneo de células madre adultas (CMA) que abarca, además de las hematopoyéticas, las endoteliales, mesenquimales (CMM), de población lateral, ovales y las progenitoras adultas multipotentes (MAPC por sus siglas en inglés). Estas últimas son CM muy pequeñas con potencialidades similares a las embrionarias. Precisamente por esta composición tan heterogénea, las células mononucleares (CMN) derivadas de la MO se consideran una especie de coctel de diferentes CMA.(3)
En Cuba el primer implante de CM de MO para tratar una enfermedad que no era hematológica se efectuó el 24 de febrero de 2004. El paciente, que padecía insuficiencia arterial crítica en la extremidad inferior derecha (con criterios de amputación mayor) fue tratado con CMN extraídas directamente de su propia MO. Para ello se le implantaron, por vía intramuscular, las CMN autólogas en los músculos gemelos de la extremidad afectada. Transcurridas 72 horas de realizado el procedimiento se constató marcada mejoría, con incrementos progresivos, y se evitó la amputación mayor.(4)
Fases del proceso de trasplante de células madre procedentes de
médula ósea
El proceso de trasplante de CM comprende varias fases consecutivas:(5) administración de agentes de movilización tales
como el factor estimulador de colonias de granulocitos (FEC-G),
movilización, extracción, preparación del producto para su
conservación y crioconservación. La última fase es la
realización, por diversas vías, del trasplante de CM (figura 2).
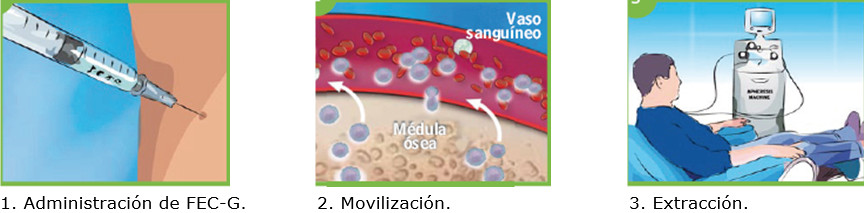

Figura 2. Proceso de trasplante de células madre(5) (modificado por el autor).
Fuente: Guía práctica para el personal de
enfermería y otros profesionales de la
atención sanitaria relacionados. European Group
for Blood and Marrow Transplantation.
En Cuba, la recogida de CM autólogas precisaba de la extracción de células de la MO de la región posterior de las crestas ilíacas del paciente, bajo anestesia general, en un quirófano hospitalario. Con la introducción de un método simplificado para extraer CM de sangre periférica (CMSP), que consiste en una técnica manual sencilla, se recolectan y procesan las CMN y las células movilizadas a la sangre periférica mediante el FEC-G, que se extraen por autodonación de sangre en un sistema cerrado de bolsas colectoras. Este procedimiento se puede hacer de manera ambulatoria y se asocia a menores tasas de morbimortalidad.(6-10)
Método simplificado para el aislamiento de células
mononucleares de sangre periférica (CMN-SP)
Inicialmente las CMN movilizadas a la sangre periférica se procesaban
y recolectaban por aféresis mediante una máquina separadora de
células. Esto fue un importante obstáculo para la extensión
del procedimiento a otras instituciones de salud, ya que pocas poseían
esta tecnología y su adquisición era significativamente costosa.
Cortina(10) diseñó un método simplificado de aislamiento de CMNSP para trasplante, a partir de su experiencia en las técnicas de bancos de sangre y trasplantes de progenitores hematopoyéticos. La movilización celular en personas que no padecen enfermedades oncológicas se realiza con citocinas (la más utilizada es el FEC-G o Hebervital®). Esta técnica es menos riesgosa para el paciente, se puede realizar de forma ambulatoria y sus efectos adversos suelen ser ligeros: cefalea, mialgias, dolor osteomuscular y ardor o dolor en el punto de inoculación del medicamento, de acuerdo con lo reportado en la literatura.
En la ejecución de este método se emplean técnicas manuales. Inicialmente se incluyó la adición de hidroxietil almidón (HES) al 6 %, para la sedimentación celular. La mezcla de la MO con HES permite agrupar los eritrocitos de forma semejante a una pila de monedas, promueve su rápida sedimentación y facilita la separación de la capa leucoplaquetaria. Posteriormente se optimizó el procedimiento (en lugar de la sedimentación celular se empleó la centrifugación celular) y fue posible obtener el concentrado más rápidamente. El método es sencillo, fácil de ejecutar y más económico que los procedimientos convencionales. El FEC-G producido en el país es de eficacia similar a los comercializados en el mercado internacional y está disponible en todas las instituciones de salud que lo requieren.(10,11)
Las CM existentes en la MO se pueden movilizar a la sangre periférica por el FEC-G. Estas células se extraen como componentes de las CMN y se les aplica el marcador CD34+ como referencia de las células madre hematopoyéticas obtenidas. Las otras células madre presentes no se tipifican. A este respecto, a varios pacientes con isquemia de extremidades inferiores se les inyectaron CMN autólogas movilizadas con FEC-G. Se comprobó que el número de CMN movilizadas resultó mejor indicador de la efectividad terapéutica que el número de células CD34+. Este dato evidencia la ventaja de emplear las CMN en su conjunto y que no es imprescindible cuantificar las células CD34+.(12)
Movilización
Las concentraciones de CMH son de 10 a 100 veces superiores en la MO, en
comparación con la circulación periférica. Por consiguiente,
se requiere incrementar las concentraciones circulantes de CMH con el fin
de asegurar extracciones adecuadas y satisfactorias. Los agentes utilizados
para movilizar las CMH son las citosinas o FEC-G, tales como el filgrastim
(Neupogen® e ior® LeukoCIM) y lenograstim (Granocyte®).(13-15)
Los FEC-G estimulan la movilización de las células madre hematopoyéticas mediante la disminución de la expresión del gen del SDF-1α y de los niveles de proteínas a la vez que aumentan las proteasas que pueden romper las interacciones entre las CMH y el ambiente de la MO (figura 3).(16)
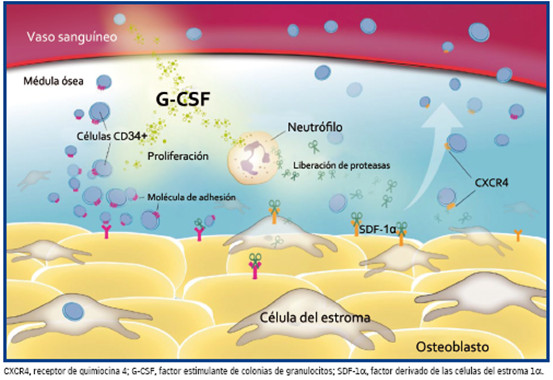
Figura 3 Mecanismo de acción del FEC-G.(5)
Fuente: Guía práctica para el personal de
enfermería y otros profesionales de la
atención sanitaria relacionados. European Group
for Blood and Marrow Transplantation.
Recientemente fue aprobado en la Unión Europea para su uso junto con el FEC-G, el plerixafor (Mozobil®). Se recomienda usar este agente en pacientes cuyas células se movilizan poco (enfermos de linfoma y mieloma múltiple), con el objetivo de movilizar las CM de la MO hacia la sangre periférica para su extracción y trasplante autólogo. El plerixafor es una molécula pequeña antagonista del CXCR4 que inhibe de manera reversible la interacción entre el CXCR4 y elSDF-1α. Se ha demostrado que el uso de plerixafor en combinación con el FEC-G mejora las extracciones de células CD34+ en los pacientes con linfoma y mieloma múltiple, en comparación con el empleo del FEC-G solo.(17,18) El Hebervital® recombinante (filgrastim) producido en Cuba por el Centro de Ingeniería Genética y Biotecnología se utiliza como agente movilizador en el sistema de salud nacional con resultados, seguridad y equivalencia terapéutica comparables al Neupogen® (considerado el producto líder a nivel internacional).
La capacidad regenerativa de las células mononucleares de la médula ósea (CMN-MO) en su conjunto, y los resultados de la administración de células mononucleares de sangre periférica (CMN-SP) autólogas movilizadas con FEC-G, fueron evaluados por Hernández Ramírez(19) como satisfactorios. Se ha planteado que la coadministración de estas células puede mejorar la regeneración de tejidos dañados debido a la acción sinérgica entre ellas. El uso de las CMN incluye todas las subpoblaciones de CM progenitoras derivadas de la MO, de cuya interrelación, balance, y coadministración puede depender una respuesta funcional más fisiológica e integral(19).
La coadministración de estas células tiene ventajas en comparación con el uso individual de la subpoblación de CM (entre ellas las CMM que han sido las más empleadas en la práctica clínica). Aunque es posible obtener las CMM de otras fuentes alternativas (tejido adiposo, sangre del cordón umbilical, músculo esquelético, dermis, membrana sinovial y pulpa dental), su manipulación es más compleja. Para ello se requiere separarlas del resto de las células presentes en el microambiente de la MO. Generalmente necesitan ser cultivadas con frecuentes cambios de medios de cultivo para su expansión. Por tanto, aumentan los riesgos de contaminación y la demora para su aplicación. Estos procedimientos requieren laboratorios con equipamiento y reactivos específicos, lo que redunda en un incremento de los costos. La demora en el procesamiento de las células puede interferir en el tratamiento oportuno de pacientes en condiciones clínicas para las que una administración terapéutica rápida pudiera dar mejores resultados (tabla 1).(20,21)
Tabla 1. Ventajas de la obtención de CMN-SP

Fuente: elaborada por los autores
Filgrastim (Hebervital®)
Los factores estimuladores de colonias hematopoyéticas se utilizan en
diferentes tratamientos médicos y actualmente se encuentran en curso
ensayos clínicos para emplearlos como adyuvantes en la mejora de los
efectos de la vacuna de la hepatitis B.(22) El FEC-G humano
recombinante es uno de los más utilizados en estudios clínicos
por diferentes laboratorios y hospitales. Este medicamento estimula la
activación, diferenciación y proliferación de las
células hematopoyéticas en el organismo, al aumentar las defensas
del huésped en respuesta a patógenos. Por otra parte tiene efecto
antiinflamatorio inmunomodulador.(23)
La movilización de las CM de la MO desde su entorno natural hacia el torrente circulatorio se realiza mediante la administración del FEC-G filgrastim (Hebervital®). Este medicamento se obtiene desde 1986 a partir de la recombinación del filgrastim en la Escherichia coli.(24,25) Su secuencia aminoacídica es idéntica a la del FEC-G humano endógeno. Solo difiere en la presencia de un residuo metionina N-terminal, necesario para la expresión del gen G-CSF en la E. coli y la ausencia de glicosilación, porque el sistema de expresión en bacterias carece de esa capacidad.(24)
La dosis recomendada para la movilización celular es de 5-10 μg/Kg de peso (en algunos casos es necesario individualizarla), por vía subcutánea o endovenosa, sin sobrepasar nunca los 1 200 µg/día. La duración del tratamiento dependerá del objetivo y la condición clínica a tratar. Se puede aplicar un esquema de movilización rápida (48 horas) o realizar una movilización más prolongada durante cinco, siete, 10 ó 15 días, en dependencia de la finalidad del tratamiento y la respuesta del paciente. Esta última se deberá evaluar periódicamente para determinar el conteo global de leucocitos, que es el parámetro de mayor valor para evaluar respuesta farmacológica.(26).
La última dosis se administrará entre tres y seis horas antes de la extracción. Previamente a la movilización, y tres horas después de última dosis de FEC-G, al paciente se le debe hacer un hemograma. Si el conteo de leucocitos es mayor de 20 x 109/L y el resto de los parámetros son normales se procede a la extracción de sangre periférica. Si es menor se continúa con la movilización hasta lograr el conteo de leucocitos antes mencionado. Se suspenderá la aplicación de FEC-G si el recuento absoluto de neutrófilos, en cualquiera de las determinaciones, sobrepasa la cifra de 90 000 cels./mm3.(26)
Administración y trasplante de células madres
Para la aplicación de las CMA presentes en la MO se pueden emplear dos
métodos generales: la movilización desde la MO hacia la sangre
periférica de CM y progenitoras hematopoyéticas y el trasplante
celular (autoinjerto). En cuanto a los procedimientos para su
ejecución, existen cinco. De ellos tres se emplean con regularidad en
los ensayos preclínicos y clínicos realizados actualmente:(27)
CONCLUSIONES
Los conocimientos actuales sobre el proceso de movilización celular, y
el método manual para la recolección y procesamiento de las
células mononucleares de la médula ósea, abren posibilidades
alentadoras en la investigación básica y clínica. Las
propiedades exclusivas de estas células y la sencillez de su
procesamiento posibilitan su utilización en el tratamiento de
diferentes enfermedades.
Conflictos de intereses
Los autores declaran que no existen conflictos de intereses.
REFERENCIAS BIBLIOGRÁFICAS
Recibido: 20 de junio de 2016
Aprobado: 15 de febrero de 2017
MsC. José Antonio Camacho Assef
Hospital General Provincial Docente "Dr. Antonio Luaces Iraola"
Calle Máximo Gómez No.257, entre 4ta y Onelio Hernández. Ciego de Ávila, Cuba. CP.65200
Correo electrónico: jac@ali.cav.sld.cu