

Informe de caso
Manifestaciones oftalmológicas de la atrofia girata de retina. Informe de caso
Ophthalmological manifestations of gyrate retinal atrophy. Case report
Manifestações oftalmológicas da atrofia retiniana girata. Relato de caso
Carlos Alberto Pérez-Padilla1*  https://orcid.org/0000-0002-2873-9291
https://orcid.org/0000-0002-2873-9291
Zaihrys del Carmen Herrera-Lazo2  https://orcid.org/0000-0002-8015-0724
https://orcid.org/0000-0002-8015-0724
Christian Xavier Mata-Chango3  https://orcid.org/0009-0009-0212-6313
https://orcid.org/0009-0009-0212-6313
1Máster en Atención Integral al Niño. Especialista de Primer Grado en Oftalmología. Subespecialista en Oftalmología Pediátrica. Profesor Titular. Universidad Regional Autónoma de Los Andes. Hospital General Docente Ambato. Ambato, Tungurahua, Ecuador.
2Máster en Atención Integral al Niño. Especialista de Primer Grado en Pediatría. Profesor Titular. Universidad Regional Autónoma de Los Andes. Hospital General Docente Ambato. Ambato, Tungurahua, Ecuador.
3Estudiante de Medicina de séptimo nivel. Universidad Regional Autónoma de Los Andes. Ambato, Tungurahua, Ecuador.
*Autor para la correspondencia. Correo electrónico:  makinario2013@gmail.com
makinario2013@gmail.com
RESUMEN
Introducción: la atrofia girata, es un trastorno metabólico raro debido a la deficiencia de la enzima ornitina aminotransferasa, de herencia autosómica recesiva, que ocasiona hallazgos corioretinianos característicos.
Objetivo: presentar el caso de una paciente afectada por atrofia girata, con énfasis en el diagnóstico, las manifestaciones oftalmológicas de la dolencia, y su tratamiento.
Presentación del caso: paciente femenina de 13 años, mestiza, residente en Ambato, provincia Tungurahua (Ecuador). Tiene antecedentes patológicos personales de atrofia girata. Acudió a la consulta por presentar disminución progresiva de la agudeza visual. En el examen de fondo de ojo se detectó atrofia hereditaria de coroides, inespecífica, desde el polo posterior hacia la periferia, en forma de anillos circulares (característicos de la enfermedad). Se le indicó un régimen dietético restrictivo en proteínas, con énfasis en la limitación de la ingesta de arginina. El protocolo de seguimiento multidisciplinario incluyó el monitoreo trimestral de los niveles de aminoácidos en plasma para ajustar las restricciones dietéticas, y la realización de exámenes semestrales para detectar precozmente complicaciones secundarias.
Conclusiones: el diagnóstico de atrofia girata de retina en esta paciente se basó en la sintomatología y el examen del fondo de ojo. El estudio genético y la detección de niveles elevados de ornitina sistémica posibilitaron confirmar el diagnóstico. El tratamiento basado en la reducción de la ingesta de arginina reduce los riesgos de agravamiento de la enfermedad. La información actualizada sobre su diagnóstico, manifestaciones oftalmológicas, y tratamiento, contribuye a llenar un vacío de conocimiento práctico.
Palabras clave: atrofia girata; coroides; fondo de ojo; retina; informes de casos; ornitina-oxo-ácido transaminasa.
ABSTRACT
Introduction: gyrate atrophy is a rare metabolic disorder due to a deficiency of the enzyme ornithine aminotransferase, inherited in an autosomal recessive manner, which causes characteristic chorioretinal findings.
Objective: to present the case of a patient affected by gyrate atrophy, with emphasis on the diagnosis, the ophthalmological manifestations of the disease, and its treatment.
Case presentation: a 13-year-old female patient, of mixed race, residing in Ambato, Tungurahua province (Ecuador). She has a personal medical history of gyrate atrophy. She attended the consultation due to progressive decrease in visual acuity. On fundoscopic examination, hereditary choroidal atrophy, of a nonspecific nature was detected, extending from the posterior pole towards the periphery, in the form of circular rings (characteristic of the disease). She was prescribed a protein-restricted diet, with an emphasis on limiting arginine intake. The multidisciplinary follow-up protocol included quarterly monitoring of plasma amino acid levels to adjust dietary restrictions, as well as semiannual examinations for the early detection of secondary complications.
Conclusions: the diagnosis of gyrate retinal atrophy in this patient was based on the symptoms and the fundus examination. Genetic testing and the detection of elevated levels of systemic ornithine confirmed the diagnosis. Treatment based on reducing arginine intake reduces the risk of disease worsening. Updated information on its diagnosis, ophthalmological manifestations, and treatment helps fill a gap in practical knowledge.
Keyworks: case reports; choroid; fundus oculi; gyrate atrophy; ornithine-oxo-acid transaminase; retina.
RESUMO
Introdução: a atrofia girata é uma doença metabólica rara causada pela deficiência da enzima ornitina aminotransferase, herdada de forma autossômica recessiva, que provoca alterações coriorretinianas características.
Objetivo: apresentar o caso de uma paciente afetada por atrofia girata, com ênfase no diagnóstico, manifestações oftalmológicas da doença e seu tratamento.
Apresentação do caso: uma paciente de 13 anos, mestiça, residente em Ambato, província de Tungurahua (Equador), apresentou antecedentes pessoais de atrofia girata. Ela procurou atendimento médico devido à diminuição progressiva da acuidade visual. O exame de fundo de olho revelou atrofia coroidal hereditária inespecífica, estendendo-se do polo posterior à periferia na forma de anéis circulares (característicos da doença). Foi prescrita uma dieta com restrição proteica, com ênfase na limitação da ingestão de arginina. O protocolo de acompanhamento multidisciplinar incluiu monitoramento trimestral dos níveis de aminoácidos plasmáticos para ajustar as restrições alimentares e exames semestrais para detectar precocemente complicações secundárias.
Conclusões: o diagnóstico de atrofia retiniana girata neste paciente foi baseado nos sintomas e no exame de fundo de olho. Os testes genéticos e a detecção de níveis elevados de ornitina sistêmica confirmaram o diagnóstico. O tratamento baseado na redução da ingestão de arginina diminui o risco de progressão da doença. Informações atualizadas sobre seu diagnóstico, manifestações oftalmológicas e tratamento ajudam a preencher uma lacuna no conhecimento prático.
Palavras chave: atrofia girata; coroide; fundo de olho; retina; relatos de casos; ornitina oxoácido transaminase.
Recibido: 16/12/2025
Aprobado: 19/01/2026
Publicado: 05/02/2026
Los tratamientos quirúrgicos de las afecciones oculares difieren en dependencia de sus causas. De ahí la importancia de contar con diagnósticos precisos antes de programar intervenciones quirúrgicas refractivas. Para ello, el oftalmólogo debe diferenciar las enfermedades según sean de orígenes inflamatorio, atópico, alérgico, distrófico o degenerativo corneal.(1) También ha de tener en cuenta la progresión de las alteraciones en la retina, causantes de disminución repentina de la agudeza visual de moderada a grave.(2)
La atrofia girata es un trastorno metabólico raro, de origen hereditario autosómico recesivo. Se debe a la deficiencia de la enzima ornitina aminotransferasa (OAT), codificada por el gen homónimo ubicado en 10q26.13 con diez axones funcionales. Esta enzima mitocondrial depende del fosfato de piridoxal (vitamina B6) y cataliza la conversión de ornitina en ácido glutámico y prolina. En los enfermos se observan lesiones coriorretinianas características.(3)
Las deficiencias enzimáticas originadas por mutaciones en el gen OAT causan concentraciones plasmáticas altas de ornitina y la progresión de las lesiones coriorretinianas características de la atrofia girata. Por ello, es vital que los pacientes asuman una dieta restringida en arginina para reducir los niveles plasmáticos de ornitina.(4)
Se debe tener en cuenta que la atrofia coriorretiniana es degenerativa y progresiva. Entre los daños observables en el examen de fondo de ojo, son características las áreas atróficas circulares coriorretinianas, claramente delimitadas y localizadas principalmente en la periferia de la retina. En pacientes de edades avanzadas las lesiones generalmente son más numerosas y de tamaños mayores, y afectan el polo posterior de la retina.(4)
Es de suma importancia que los especialistas en oftalmología estén capacitados para diagnosticar y tratar esta enfermedad rara, que ocasiona complicaciones graves durante su evolución. Por ello, el objetivo de este artículo es presentar el caso de una paciente afectada por atrofia girata, con énfasis en el diagnóstico, las manifestaciones oftalmológicas de la dolencia, y su tratamiento.
INFORMACIÓN DEL PACIENTE
Paciente femenina de 13 años, mestiza, residente en Ambato, provincia Tungurahua (Ecuador). Tiene antecedentes patológicos personales de atrofia girata, y acudió a la consulta externa de oftalmología por presentar disminución progresiva de la agudeza visual.
Durante la anamnesis refirió que no sufría dolor ni otros síntomas. En el examen de fondo de ojo (Fig. 1) se detectó atrofia hereditaria de coroides, inespecífica, desde el polo posterior hacia la periferia, en forma de anillos circulares (característicos de la atrofia girata).

Fig. 1 - Fotografía a color del fondo de ojo. Obsérvense las áreas atróficas coriorretinianas, nítidas en la periferia.
Los familiares de la paciente expresaron su conformidad para la publicación del caso, mediante la firma del documento de consentimiento informado. El Comité de Ética de la institución hospitalaria, aprobó el presente artículo científico.
La paciente cooperó con los especialistas durante los procedimientos diagnósticos de su enfermedad. Tanto ella como sus familiares quedaron satisfechos con la atención recibida.
Durante el examen físico de la paciente, sus mucosas estaban húmedas. En la revisión del aparato respiratorio se escuchó murmullo vesicular conservado, sin ruidos sobreañadidos; la frecuencia respiratoria fue de 20 respiraciones por minuto. Los ruidos cardíacos fueron rítmicos, de buen tono e intensidad; no se identificaron soplos. La frecuencia cardíaca fue de 84 pulsaciones por minuto, y la tensión arterial de 118/79 mm Hg.
Las arcadas dentarias superior e inferior estaban completas, la lengua limpia, el abdomen suave y depresible; no se detectó visceromegalia. Se notaron ruidos hidroaéreos. El reconocimiento del sistema nervioso evidenció que la paciente estaba orientada en el tiempo y el espacio; no presentó alteraciones de la marcha ni el lenguaje, como tampoco signos meníngeos.
A la paciente se le indicaron los exámenes de rigor: fondo de ojo, campo visual, pericampimetría, y control respectivo. Se comprobó la degeneración periférica de la retina, causada por la atrofia girata, la que a su vez disminuye de forma progresiva con los años. La valoración oftalmológica fue integral, para confirmar el diagnóstico y evaluar la progresión de la enfermedad.
En el fondo de ojo se observaron áreas circulares múltiples de atrofia coriorretiniana (Fig. 1), bien delimitadas, con bordes festoneados confluyentes, localizadas desde la periferia media hacia el polo posterior. Se vieron los vasos coroideos subyacentes, y palidez papilar relativa (Fig. 2).
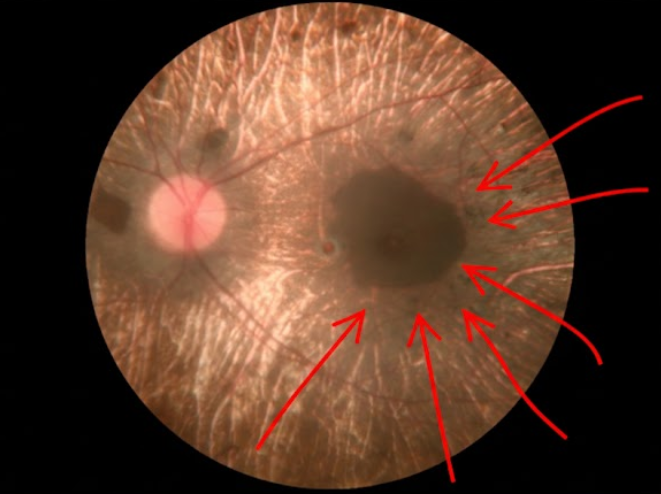
Fig. 1- Fotografía a color del fondo de ojo. Obsérvese la atrofia de la retina, en forma de anillo (señalado por las flechas rojas), característica de la enfermedad.
Los resultados de los exámenes de campo visual y pericampimetría revelaron estrechamiento concéntrico significativo del campo visual (tubular), con escotomas anulares relacionados directamente con las áreas de atrofia observadas en la fundoscopia. La visión periférica estaba limitada de forma grave, y la paciente conservaba únicamente una pequeña isla de visión central.
La atrofia girata aparece a partir de la deficiencia funcional de la enzima OAT; por tanto, el tratamiento a la paciente se centró en la reducción de los niveles plasmáticos de ornitina para limitar la progresión de la degeneración coriorretiniana. Se le indicó un régimen dietético restrictivo en proteínas, con énfasis en la limitación de la ingesta de arginina (precursor directo en la síntesis de ornitina), de modo que se evite el agravamiento de las lesiones oculares y se preserve la visión residual.
Como complemento, se inició una prueba terapéutica con clorhidrato de piridoxina en dosis de 300 mg diarios. El objetivo fue identificar si la paciente era sensible a la vitamina B6, ya que este cofactor potencia la actividad residual de la enzima OAT, y posibilita reducir significativamente la hiperornitinemia.
A la par, se estableció un protocolo de seguimiento multidisciplinario a la paciente, mediante el monitoreo trimestral de los niveles de aminoácidos en plasma para ajustar las restricciones dietéticas. Desde la perspectiva oftalmológica, cada seis meses a la paciente se le realizarán campimetría computarizada y tomografía de coherencia óptica, para detectar precozmente complicaciones secundarias como el edema macular cístico, y documentar la estabilidad de las áreas de atrofia observadas en las imágenes diagnósticas.
La ornitina se deposita en varios tejidos corporales; las manifestaciones características de esa acumulación son miopía, cataratas, atrofia coriorretiniana progresiva, y cambios maculares. De ahí que los pacientes padezcan ceguera nocturna, reducción del campo visual, disminución de la agudeza visual central, y ceguera.(5) El tratamiento dietético restringido en arginina, o la administración de vitamina B6 (precursora de la coenzima piridoxal fosfato), limitan la carga de ornitina.(6)
Aún no se conocen con exactitud los mecanismos moleculares por los cuales el déficit de OAT ocasiona daños retinianos.(6) Sin embargo, se conoce que debido a la deficiencia de esta enzima las concentraciones en plasma del aminoácido ornitina aumentan entre 10 y 20 veces en comparación con los nieles plasmáticos normales; por lo cual se le atribuyen las manifestaciones oculares de la enfermedad.(7)
El aspecto característico del fondo de ojo (coroideremia) es uno de los daños apreciables precozmente en los pacientes. Consiste en concentraciones de pigmento en el epitelio pigmentario de la retina, y atrofia peripapilar. De ahí que en la etapa avanzada de la enfermedad, la pérdida del epitelio pigmentario retiniano y coriocapilar origine áreas festoneadas confluentes semejantes a las observadas en etapas posteriores de la atrofia girata.(8-10) Estos pacientes padecen desde la infancia de disminución de la agudeza visual, asociada a ceguera nocturna y visión periférica deficiente.
La atrofia girata de la coroides y la retina es secundaria a la deficiencia de OAT. Esta carencia no se diagnostica de forma frecuente en la infancia, por lo cual los pacientes desarrollan miopía y la degeneración retiniana característica acompañada de hiperornitinemia. Ello es indicio de que en la primera infancia aparecen hiperamonemia, encefalopatía, y un perfil bioquímico caracterizado por la ornitina plasmática baja, con citrulina y arginina, y aumentos de la excreción urinaria de homocitrulina y ácido orótico (similar a un trastorno del ciclo de la urea).(11)
La atrofia girata aparece en la primera década de la vida, con una razón proporcional de 8 x 100 casos entre los hombres y 10 x 100 entre las mujeres.(12) En la mayoría de los enfermos el diagnóstico se efectúa o confirma a partir de los ocho años de edad. De su precocidad depende, en razón directamente proporcional, el éxito del tratamiento. Los hallazgos oftalmológicos característicos de la atrofia aparecen a partir de los seis años; aproximadamente 30 % de los pacientes diagnosticados desarrollan edema macular, y 60 % cataratas preseniles.(13)
Las variantes de la atrofia girata dependen de la patogenenicidad del gen OAT en los pacientes portadores. Ello significa que pueden aparecer variantes de la OAT (c.G248A; p.S83) homólogas y perjudícales, que contribuyan a la progresión de la enfermedad.(14) Si esas variedades se repiten en cada uno de los individuos de una familia, las imágenes retinianas y los análisis metabólicos de pedigríes de matrimonios consanguíneos pueden servir de guías para diagnosticar y tratar con precisión la enfermedad.
El diagnóstico más certero se basa tanto en el examen físico, particularmente la revisión del fondo de ojo (en el cual se observan las lesiones características debidas a la hiperornitinemia plasmática), como en la detección de mutaciones en el gen de la enzima OAT.(15,16) El reconocimiento temprano y el tratamiento adecuado de la atrofia girata son indispensables para frenar la pérdida brusca y repentina de la agudeza visual. Debido a las complicaciones frecuentes de esta enfermedad, se deben utilizar modalidades terapéuticas adyuvantes peri y posoperatorias, y seguir en consulta de forma regular el estado de los pacientes.(17-19)
En la actualidad no existe una terapia génica eficaz, debido que la atrofia girata es una enfermedad rara. El tratamiento habitual consiste principalmente en modificaciones dietéticas restrictivas de la arginina (con suplementos de piridoxina, lisina, o creatina). El objetivo es reducir la ingesta de arginina en cuanto precursor de ornitina.(20-22)
En experimentos ex vivo preliminares se ha comprobado que los glóbulos rojos cargados con la enzima OAT pueden metabolizar la ornitina extracelular en concentraciones similares a las encontradas en los pacientes, tanto en el plasma como en la irrigación sanguínea. Por ello, pudiera esperarse que un tratamiento mediado por glóbulos rojos es factible como un nuevo enfoque terapéutico para esta enfermedad.(23)
Este trabajo se vio limitado en cuanto a la carencia de bibliografía en español y datos concretos de la incidencia de la atrofia girata de retina, debido a su rareza.
El diagnóstico de atrofia girata de retina en esta paciente se basó en la sintomatología y el examen del fondo de ojo. El estudio genético y la detección de niveles elevados de ornitina sistémica posibilitaron confirmar el diagnóstico. El tratamiento basado en la reducción de la ingesta de arginina reduce los riesgos de agravamiento de la enfermedad. La investigación aportó evidencias científicas valiosas sobre una afección rara, desconocida en la práctica por muchos especialistas. La información actualizada sobre su diagnóstico, manifestaciones oftalmológicas, y tratamiento, contribuye a llenar ese vacío de conocimiento práctico.
1. Albé E, Tassignon MJ. Enfermedades oculares de importancia en cirugía refractiva. Cirugía Refractiva. 2da ed. Ámsterdam: Elsevier; 2020. p. 132-145.
2. Salmon JF. Distrofias hereditarias del fondo de ojo. En: Kanski: Oftalmología clínica. Un enfoque sistemático. 9ª ed. Barcelona, España: Elsevier España, S.L.U.; 2021. p. 488-532.
3. Çavdarlı C, Şahlı E, Çavdarlı B, Numan M. "Regression of macular edema with topical brinzolamide and nepafenac alone and identification of a novel gyrate atrophy mutation." Arq Brasil Oftalmol [Internet]. 2020 [citado 4 Oct 2025];83(2):149-52. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC11826744/pdf/abo-83-02-0149.pdf
4. Jalali H, Najafi M, Khoshaeen A, Mohammad-Reza M, Mahdavi M. "First report of c. 425-1G> A mutation in ornithine aminotransferase gene causing gyrate atrophy of the choroid and retina with hyperornithinemia." Eur J Ophthalmol [Internet]. 2021 [citado 4 Oct 2025];31(5):NP23-NP26. Disponible en: https://pubmed.ncbi.nlm.nih.gov/32418451/
5. Mejía-Alvarán M. y Ortiz-Zapata AI. Interpretación campimétrica. En: Neuropatías ópticas de la A a la Z. Barcelona, España: Elsevier; 2024:121.
6. Montioli R, Bellezza I, Desbats MA, Borri-Voltattorni C, Salviati L, Cellini B. Deficit of human ornithine aminotransferase in gyrate atrophy: Molecular, cellular, and clinical aspects. Biochim Biophys Acta Proteins Proteom [Internet]. 2021 [citado 4 Oct 2025];1869(1):140555. Disponible en: https://www.sciencedirect.com/science/article/abs/pii/S1570963920302028
7. Elnahry AG, Tripathy K. Gyrate Atrophy of the Choroid and Retina. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 [citado 4 Oct 2025]. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK557759/
8. Balfoort BM, Pampalone G, Ruiter JPN, Denis SW, Brands MM. Extending diagnostic practices in gyrate atrophy: Enzymatic characterization and the development of an in vitro pyridoxine responsiveness assay. Mol Genet Metab [Internet]. Sep-Oct 2024 [citado 4 Oct 2025];143(1-2):108542. Disponible en: https://www.sciencedirect.com/science/article/pii/S1096719224004268
9. Elnahry AG, Elnahry GA. Rotated atrophy of the choroid and retina: a review. Eur J Ophthalmol [Internet]. 2022 [citado 4 Oct 2025];32(3):1314-23. Disponible en: https://journals.sagepub.com/doi/10.1177/11206721211067333?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
10. Labiano AT, Arroyo MH. Gyrate atrophy-like phenotype with normal plasma ornithine and low plasma taurine. GMS Ophthalmol Cases [Internet]. Feb 27 2020 [citado 4 Oct 2025];10:1-5. Disponibe en: https://pmc.ncbi.nlm.nih.gov/articles/PMC7113615/pdf/OC-10-04.pdf
11. Kaczmarczyk A, Baker M, Diddle J, Yuzyuk T, Valle D, Lindstrom K. A neonate with ornithine aminotransferase deficiency; insights on the hyperammonemia-associated biochemical phenotype of gyrate atrophy. Mol Genet Metab Rep [Internet]. Mar 2022 [citado 4 Oct 2025];16(31):100857. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC9248225/pdf/main.pdf
12. Pauleikhoff L, Weisschuh N, Lentzsch A, Spital G, Krohne TU, Agostini H, et al. Clinical characteristics of gyrate atrophy compared with a gyrate atrophy-like retinal phenotype. Eur J Ophthalmol [Internet]. Jan 2024 [citado 4 Oct 2025];34(1):79-88. Disponible en: https://journals.sagepub.com/doi/10.1177/11206721231178147?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
13. Palmer E, Stepien KM, Campbell C, Barton S, Iosifidis C, Ghosh A, et al. Clinical, biochemical and molecular analysis in a cohort of individuals with gyrate atrophy. Orphanet J Rare Dis [Internet]. 4 Sep 2023 [citado 4 Oct 2025];18(1):265. Disponible en: https://pmc.ncbi.nlm.nih.gov/articles/PMC10476330/pdf/13023_2023_Article_2840.pdf
14. Huang J, Fu J, Fu S, Yang L, Nie K, Duan C, et al. Diagnostic value of a combination of next-generation sequencing, chorioretinal imaging and metabolic analysis: lessons from a consanguineous Chinese family with gyrate atrophy of the choroid and retina stemming from a novel OAT variant. Br J Ophthalmol [Internet]. Mar 2019 [citado 4 Oct 2025];103(3):428-35. Disponible en: https://bjo.bmj.com/content/103/3/428.long
15. da Palma MM, Ku C, Igelman AD, Burr A, Shevchenko-Sutherland L. A possible ocular biomarker for response to hyperornithinemia in gyrate atrophy: the effect of pyridoxine, lysine, and arginine-restricted diet in a patient with advanced disease. Ophthalmic Genet [Internet]. Apr 2023 [citado 4 Oct 2025];44(2):191-7. Disponible en: https://www.tandfonline.com/doi/10.1080/13816810.2022.2098986?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
16. Merino-Diez MT, Soria-Prada C, Zamorano-Aleixandre M, Gonzalez-Lopez JJ. "Gyrate atrophy of the choroid and retina: Update on diagnosis and treatment. Arch Soc Esp Oftalmol (Engl Ed) [Internet]. 2024 [citado 4 Oct 2025];99(9):392-9. Disponible en: https://www.sciencedirect.com/science/article/abs/pii/S2173579424000719
17. Ozcaliskan S, Balci S, Artunay O. A Case of Foveoschisis Associated with Ornithine Aminotransferase Deficiency and Gyrate Atrophy. J Coll Physicians Surg Pak [Internet]. 2021 Nov [citado 4 Oct 2025];31(11):1354-6. Disponible en: https://www.jcpsp.pk/oas/mpdf/generate_pdf.php?string=dTJmR2pzTEpuSVQ2Tjh6T3N2cktzZz09
18. Berhuni M, Tıskaoğlu NS. Foveoschisis associated with gyrate atrophy in ornithine aminotransferase deficiency: A case report. Photodiagnosis Photodyn Ther [Internet]. Jun 2023 [citado 4 Oct 2025];42:103618. Disponible en: https://www.sciencedirect.com/science/article/abs/pii/S1572100023003459?via%3Dihub
19. Castaño-Silos JC, Sanchez-Guillen I, Almorín-Fernández-Vigo I, Jerez-Fidalgo M, Fernández-Vigo JI. Atrofia coriorretiniana pigmentada paravenosa de presentación unifocal y unilateral. Arc Soc Esp Oftalmol [Internet]. Abr 2023 [citado 4 Oct 2025];98(4):233-7. Disponible en: https://www.sciencedirect.com/science/article/abs/pii/S0365669123000011
20. Ju Y, Zong Y, Li X, Gao F, Chang Q, Huang X. Mild Phenotypes of Gyrate Atrophy in a Heterozygous Carrier with One Variant Allele of OAT. Genes (Basel) [Internet]. Ago 2024 [citado 4 Oct 2025];15(8):1020. Disponible en: https://www.mdpi.com/2073-4425/15/8/1020
21. Pires-Franco de Oliveira BA, Vieira-Bussad M, Peyneau-Poncio L, Delpupo-Moro N. Atrofia girata da coroide e retina: atualização sobre diagnóstico e tratamento. Archives of Health, Curitiba [Internet]. 2025 [citado 4 Oct 2025];6(4):1-6. Disponible en: https://ojs.latinamericanpublicacoes.com.br/ojs/index.php/ah/article/view/3413/3117
22. Balfoort BM, Buijs MJN, Ten-Asbroek AL, Bergen AA, Boon CJ, Ferreira EA, et al. A review of treatment modalities in gyrate atrophy of the choroid and retina (GACR). Mol Genet Metab [Internet]. Sep-Oct 2021 [citado 4 Oct 2025];134(1-2):96-116. Disponible en: https://www.sciencedirect.com/science/article/pii/S1096719221007629?via%3Dihub
23. Pampalone G, Chiasserini D, Pierigè F, Camaioni E, Orvietani PL, Bregalda A, et al. Biochemical Studies on Human Ornithine Aminotransferase Support a Cell-Based Enzyme Replacement Therapy in the Gyrate Atrophy of the Choroid and Retina. Int J Mol Sci [Internet]. Jul 2024 [citado 4 Oct 2025];25:7931. Disponible en: https://pdfs.semanticscholar.org/d8cf/757a8c869b577e8e411f0e0ffea9a47f2822.pdf
Conflicto de intereses
Los autores declaran que no existen conflictos de intereses.
Contribución de los autores
Carlos Alberto Pérez-Padilla: conceptualización, investigación, metodología, administrador del proyecto, recursos, supervisión, validación, visualización, redacción del borrador original, redacción, revisión y edición.
Zaihrys del Carmen Herrera-Lazo: adquisición de fondos, investigación, recursos, supervisión, visualización y redacción, revisión y edición.
Christian Xavier Mata-Chango: análisis formal, investigación, metodología, software, visualización y redacción revisión y edición.
Financiación
Hospital General Docente Ambato. Ambato, Tungurahua, Ecuador.
 Esta obra está bajo una licencia internacional Creative Commons Attribution4.0/International/Deed.
Esta obra está bajo una licencia internacional Creative Commons Attribution4.0/International/Deed.