
CIEGO DE ÁVILA
ISSN: 1029-3035
RNPS: 1821

Publicación Trimestral de la Universidad de Ciencias Médicas de Ciego de Ávila Editorial Ciencias Médicas |
|||
 |
REVISTA MÉDICA ELECTRÓNICA DE CIEGO DE ÁVILA |
2020;26(1):e1125 ISSN: 1029-3035 RNPS: 1821 |
 |

Presentación de caso
Elevada supervivencia en paciente con cáncer de pulmón avanzado tratada con Vaxira®
High survival in a patient with advanced lung cancer treated with Vaxira®
Tatiana Hernández-Casola1* https://orcid.org/0000-0002-1237-0610
Yixi Pérez-Morales2 https://orcid.org/0000-0002-7204-1448
Thayde Trujillo-Tirado3 https://orcid.org/0000-0002-3755-0204
1Máster en Urgencias Médicas. Licenciada en Enfermería. Profesor Asistente. Hospital General Docente “Cptan. Roberto Rodríguez Fernández”, Morón. Ciego de Ávila, Cuba.
2Especialista de Primer Grado en Oftalmología y Medicina General Integral. Profesor Asistente. Hospital General Docente “Cptan. Roberto Rodríguez Fernández”, Morón. Ciego de Ávila, Cuba.
3Máster en Toxicología Experimental. Licenciada en Ciencias Farmacéuticas. Profesor Auxiliar. Centro Nacional de Ensayos Clínicos. La Habana, Cuba.
* Autor para la correspondencia. Correo electrónico: rmonzon@infomed.sld.cu
RESUMEN
Introducción: el cáncer de pulmón se considera el tumor maligno que más muertes produce en el mundo por encima de otros cánceres con mayor incidencia en la población general, como el de colon o el de mama, ya que su detección en etapas tempranas es difícil y en el 90 % de los casos se diagnostica en estadios avanzados, cuando el tratamiento ya no es tan eficaz. En Cuba, el cáncer constituye la segunda causa de muerte; los tumores de tráquea, bronquios y pulmón son los de mayor incidencia.
Objetivo: presentar el caso de una paciente con cáncer de pulmón avanzado que tuvo una supervivencia mayor que la esperada para esta etapa de la enfermedad.
Presentación del caso: paciente femenina, de 70 años de edad, con diagnóstico citohistológico de carcinoma de pulmón de células no pequeñas, etapa IV, que recibió tratamiento oncoespecífico de primera línea con quimioterapia y radioterapia, después fue incluida en el Ensayo Clínico RANIDO fase III, en el grupo racotumomab; la supervivencia de la paciente fue de 32 meses al diagnóstico y de 25 meses a la inclusión en el ensayo clínico.
Conclusiones: en el caso de esta paciente con cáncer de pulmón de células no pequeñas en estadio avanzado, la administración de la vacuna racotumomab incrementó su supervivencia, comparado con lo referido en la literatura revisada.
Palabras clave: NEOPLASIAS PULMONARES/tratamiento farmacológico; CARCINOMA DE PULMÓN DE CÉLULAS NO PEQUEÑAS/tratamiento farmacológico; VACUNAS CONTRA EL CÁNCER/uso terapéutico; SUPERVIVENCIA; INFORMES DE CASOS.
ABSTRACT
Introduction: lung cancer is considered the malignant tumor that produces the most deaths in the world over other cancers with higher incidence, such as colon or breast cancer, since its detection in early stages is difficult and in 90 % of cases it is diagnosed in advanced stages, when treatment is no longer as effective. In Cuba, cancer constitutes the second cause of death. Tracheal, bronchial, and lung tumors are the ones with the highest incidence.
Objective: to present the case of a patient with advanced lung cancer who had a higher survival than expected for this stage of the disease.
Case presentation: a 70-year-old female patient with a cytohistological diagnosis of non-small cell lung carcinoma, stage IV, who received first-line oncospecific treatment with chemotherapy and radiotherapy, was then included in the RANIDO Phase III Clinical Trial, in the racotumomab group; patient survival was 32 months at diagnosis and 25 months at inclusion in the clinical trial.
Conclusions: in the case of this patient with advanced stage non-small cell lung cancer, the administration of the racotumomab vaccine increased her survival, compared to that reported in the reviewed literature.
Keywords: NON-SMALL-CELL LUNG CARCINOMA/drug therapy; LUNG NEOPLASMS/drug therapy; CANCER VACCINES/ /therapeutic use; SURVIVORSHIP; CASE REPORTS.
Recibido: 11/06/2018
Aprobado: 04/12/2019
INTRODUCCIÓN
Según la Organización Mundial de la Salud (OMS) cada hora se diagnostican 1 500 personas con cáncer en el mundo y fallecen más de 22 000; el de pulmón es uno de los tipos más comunes.(1) El cáncer de pulmón se considera el tumor maligno que más muertes produce en el mundo, por encima de otros cánceres con mayor incidencia en la población general como el de colon o el de mama, ya que su detección en etapas tempranas es difícil; en 90 % de los casos se diagnostica en estadios avanzados cuando el tratamiento ya no es tan eficaz.(2) Se estimó que para el año 2020 habría 9 000 000 de casos nuevos en los países en vías de desarrollo y 6 000 000 en las naciones desarrolladas; la OMS prevé que para el 2030 lo presentarán 17 000 000 de habitantes en el planeta.(3)
En Cuba, el cáncer constituye la segunda causa de muerte; los tumores de tráquea, bronquios y pulmón son los de mayor incidencia, han ocasionado un total de 24 345 muertes en 2016, 25 232 en 2017 y 24 902 en 2018. En la provincia Ciego de Ávila el cáncer representó la primera causa de muerte en los años 2016, 2017 y 2018.(4-6) En esta provincia los tumores de tráquea, bronquios y pulmón representaron 28,9 % de las muertes por cáncer en 2016, 25,5 % en 2017 y 21 % en 2018.(7)
El cáncer de pulmón de células no pequeñas (CPCNP) es el subtipo más frecuente en la población, representa 75 % de todos los tumores pulmonares. Tiene un pronóstico desfavorable (solo 16 % de los pacientes sobreviven a los cinco años) por la baja efectividad de los tratamientos y el desarrollo de resistencia tumoral intrínseca y adquirida.(8)
El objetivo del tratamiento del cáncer es permitir a los pacientes vivir durante el mismo tiempo y con la misma calidad de vida que si no tuvieran la enfermedad. Las quimioterapias se han convertido en un procedimiento indispensable para la reducción de la carga tumoral y el aumento de la supervivencia, pero su impacto en el cáncer de pulmón solo es medible en meses, con graves reacciones adversas como perjuicio adicional.(9) Se ha reportado una mediana de supervivencia posquimioterapia basada en platino de 3,17 meses para la etapa IV de la enfermedad.(10) Estudios realizados en Santiago de Cuba y Granma reportan una supervivencia de 13 y ocho meses, respectivamente, para todos los pacientes con cáncer de pulmón de células no pequeñas, independientemente del estadio de la enfermedad.(11-12)
El mecanismo de acción de los anticuerpos monoclonales y de las vacunas terapéuticas es mucho más selectivo en la eliminación de las células tumorales y puede aumentar la supervivencia de los pacientes con mejor calidad de vida.(13) Racotumomab es una vacuna terapéutica contra el cáncer destinada al tratamiento de los tumores de pulmón y mama, y los melanomas.(14)
La presentación del caso está motivada por la evolución favorable de una paciente con cáncer de pulmón de células no pequeñas avanzado, tratada con quimioterapia y radioterapia, y posteriormente con la vacuna racotumomab, que tuvo un tiempo de supervivencia superior a lo esperado para esta etapa de la enfermedad.
PRESENTACIÓN DEL CASO
Paciente femenina, blanca, de 70 años, fumadora, con antecedentes de diabetes mellitus y enfermedad pulmonar obstructiva crónica, que acudió al Servicio de Medicina Interna del Hospital General Docente “Cptan. Roberto Rodríguez Fernández”, por presentar disnea, astenia, anorexia, fiebre de cinco días de evolución (hasta 39,5 oC), tos húmeda productiva con expectoración blanquecina y mucosanguinolenta.
Examen físico:
La paciente, durante el examen físico general, mostró aspecto de enferma, con palidez y tejido celular subcutáneo infiltrado en ambos miembros inferiores. En cuanto al sistema respiratorio se observó disnea moderada y frecuencia respiratoria de 24 por minuto, y murmullo vesicular disminuido en la base pulmonar izquierda, con estertores húmedos. En el sistema cardiovascular se constató una frecuencia cardíaca de 104 latidos por minuto, tensión arterial de 150/100 mm Hg. El resto de los sistemas se mostraron normales.
Estudio imagenológico:
Se realizó a la paciente un topograma de tórax 1 (Fig. 1), en el cual se observó opacidad total del lóbulo superior izquierdo, con solo un segmento de la base de ese lóbulo (superior) que mostró transparencia heterogénea por trama reforzada del segmento libre, además de opacidad total del lóbulo inferior que aumentaba en sentido cráneocaudal, y ensanchamiento de los espacios intercostales a ese nivel; aspecto de derrame pleural y ligero desplazamiento del mediastino hacia el lado sano.
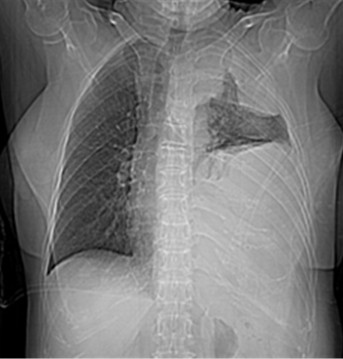
Fig. 1 - Topograma de tórax al momento del diagnóstico.
Se observaron el hemitórax derecho de transparencia normal y el seno costofrénico libre. El ultrasonido abdominal mostró un resultado normal.
La tomografía axial computarizada (TAC) de pulmón monocorte a 10 mm simple y contrastada mostró una imagen hiperdensa en el lóbulo superior izquierdo, de localización posterior, que tiene captación del medio de contraste de contornos espiculados, de 53 x 40 mm; así como una imagen hiperdensa de 24 x 18 mm adosada a la pleura, que produce destrucción costal del lado izquierdo, trama broncovascular acentuada, derrame pleural de mediana a gran cuantía y adenopatía paratraqueal de 13 mm de diámetro menor.
Estudio anatomopatológico:
Se realizó una biopsia por aspiración con aguja fina (BAAF) de pulmón con lo que se constató la presencia de un carcinoma de pulmón de células no pequeñas, lo que sugiere la presencia de carcinoma epidermoide moderadamente diferenciado; se clasificó su estado como etapa IV (T2N2M1b).
Se inició el tratamiento de primera línea para la enfermedad oncológica, para el que se planificaron cuatro ciclos de carboplatino/vinblastina y radioterapia con una dosis total diaria de dos Gy, para una dosis total del tratamiento de 60 Gy.
La paciente se evaluó un mes después de concluir el tratamiento oncoespecífico de primera línea como respuesta parcial y se decidió proponerle la inclusión en el “Ensayo Clínico multicéntrico, aleatorizado, estratificado, abierto y comparado en pacientes con cáncer de pulmón de células no pequeñas en estadios avanzados tratados con racotumumab o nimotuzumab vs docetaxel después de la primera línea de tratamiento oncoespecífico” (RANIDO). La paciente aceptó participar en el estudio, expresando su voluntariedad mediante la firma el consentimiento informado, se aleatorizó e incluyó en el grupo racotumomab.
Se le administró la vacuna racotumomab (1 mg por vía intradérmica); las cinco primeras dosis cada 14 días (etapa de inducción) y el resto (etapa de mantenimiento) cada 28 días, hasta que ocurrió un deterioro clínico que provocó la interrupción del tratamiento, alrededor de 23 meses después de haberlo iniciado.
Se le realizaron exámenes de laboratorio e imagenológicos antes de incluirla en el estudio para la evaluación inicial, y después cada tres meses hasta completar los 24; los resultados se describen a continuación.
Al realizar la evaluación inicial para el ensayo clínico, en la TAC se observó una imagen en el lóbulo superior del pulmón izquierdo de 34 mm en su diámetro mayor y la desaparición de la imagen adosada a la pleura. El examen físico muestró resultados normales. La respuesta al tratamiento oncoespecífico de primera línea fue parcial. Los exámenes complementarios mostraron resultados hematológicos y de química sanguínea normales, excepto la lactato deshidrogenasa (LDH) y la gamma glutamil transferasa (GGT), que estaban elevadas.
Al realizar la evaluación a los tres meses de haber iniciado el tratamiento con racotumomab, en la TAC se observó en el lóbulo superior del pulmón izquierdo una imagen de 20 mm, que se concluyó era una respuesta parcial al tratamiento, debido a la disminución de 41 % de su tamaño con respecto a la evaluación inicial del ensayo clínico. El examen físico de todos los sistemas resultó normal, así como el examen hematológico. En la química sanguínea solamente la GGT se encontraba elevada.
En la evaluación a los 12 meses, en la TAC se constató que había desaparecido la imagen del lóbulo superior del pulmón izquierdo, lo que se consideró respuesta completa al tratamiento. Los exámenes físico y hematológico tuvieron valores normales; en la química sanguínea se encontraron elevadas la fosfatasa alcalina y la GGT, además de la glucemia.
En la evaluación a los 15 meses, en la TAC volvió a observarse una imagen de 34 mm en el lóbulo superior izquierdo (Fig. 2), lo que indicó un progreso la enfermedad. En el examen físico se observó tejido celular subcutáneo infiltrado en ambos miembros inferiores hasta la rodilla, murmullo vesicular conservado y estertores roncos aislados. En el examen hematológico el conteo de plaquetas estaba por debajo de los valores normales, el resto se encontró normal. El análisis de la química sanguínea mostró valores elevados de la fosfatasa alcalina, la GGT y la glucemia.
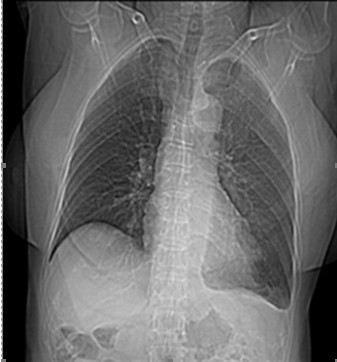
Fig. 2 - Topograma de tórax 15 meses después de iniciado el tratamiento con racotumomab.
Al realizar la evaluación a los 24 meses, en la TAC se observó una imagen de 38 mm en el lóbulo superior izquierdo. El examen físico mostró la misma sintomatología que en la evaluación correspondiente a los 15 meses; el examen hematológico dio resultados normales y en la química sanguínea se mantenían elevadas la fosfatasa alcalina y la GGT.
La paciente recibió un total de 26 inmunizaciones con la vacuna racotumomab. La supervivencia global fue de 32 meses al diagnóstico y de 25 meses después de la administración de racotumomab. Durante la administración de la vacuna no presentó eventos adversos graves, solo locales en el sitio de administración del medicamento, y otros relacionados con la progresión de la enfermedad.
DISCUSIÓN
El CPCNP es el tipo de cáncer de pulmón más frecuente y representa 80 % de todos los diagnósticos de cáncer de este órgano. La tasa de supervivencia a los cinco años en pacientes con esta enfermedad es de 23 %. Si el cáncer se ha diseminado a partes distantes del cuerpo, lo que se denomina cáncer de pulmón metastásico, la tasa de supervivencia a los cinco años es de 6 %.(15) Los nuevos productos biológicos incorporados al arsenal terapéutico constituyen las herramientas para convertir al cáncer en una enfermedad crónica, no transmisible y compatible con años de calidad de vida.(16)
Antes de iniciarse, el ensayo clínico RANIDO fue evaluado y aprobado por el Comité de Ética para la Investigación del Hospital General Docente “Cptan. Roberto Rodríguez Fernández”; además, la paciente otorgó el consentimiento informado para su participación en el estudio, lo que evidencia el cumplimiento de las normas éticas para investigaciones en seres humanos.
El tiempo de supervivencia en este caso se aproxima a lo reportado en una guía de referencia rápida mexicana de 2019, donde la sobrevida para el CPCNP en estadio IVb es de 10 % a los 24 meses y de 0 % a los 60 meses.(17) En Zaragoza, España, se encontró una media de supervivencia de 25,74 meses para los pacientes tratados en un hospital de referencia.(18)
En un estudio realizado en Santiago de Cuba se reporta que la mediana de supervivencia de los pacientes con CPCNP atendidos en el Servicio de Oncología del Hospital Provincial Docente Clínico Quirúrgico "Saturnino Lora Torres" es de 13 meses, independientemente del estadio en que se diagnosticó la enfermedad.(11) En otro estudio realizado en Granma se encontró un promedio de supervivencia de 240,83 días (alrededor de ocho meses).(12) La paciente reportada en el presente trabajo tuvo una supervivencia superior a lo reportado en estas provincias de Cuba.
Otros artículos refieren que la mediana de supervivencia para los pacientes con CPCNP es de aproximadamente 11 meses después del diagnóstico, aunque reciban todas las líneas de terapia oncoespecíficas convencionales. Además, se ha reportado una mediana de supervivencia posquimioterapia basada en platino de 4,93 meses para la etapa IIIB y 3,17 para la etapa IV.(10-11)
La vacuna racotumomab induce al sistema inmunológico del paciente a generar una respuesta contra un blanco molecular específico del cáncer, con el fin de controlar el crecimiento del tumor, retrasar el avance de la enfermedad y por consiguiente, aumentar la sobrevida del paciente.(14) Un estudio realizado por el Centro de Inmunología Molecular refiere una mediana de supervivencia global de 12,3 meses en el grupo tratado con la vacuna racotumomab.(19-20) La supervivencia del caso estudiado también fue superior a este reporte.
A la paciente estudiada no se le realizó cuantificación de la concentración basal de EGF, cuyo valor pudiera estar relacionado con la supervivencia observada en este caso, ya que la concentración de EGF circulante en el suero basal, es un posible biomarcador con valor pronóstico y predictivo de la supervivencia en pacientes con CPCNP,(22) lo cual constituye una limitación en este estudio.
En el caso estudiado, la administración de la vacuna racotumomab incrementó la supervivencia de la paciente con cáncer de pulmón de células no pequeñas en estadio avanzado, comparado con lo referido en la literatura revisada.
REFERENCIAS BIBLIOGRÁFICAS
Conflictos de intereses
Los autores declaran que no existen conflictos de intereses.
Contribuciones de los autores
Tatiana Hernández-Casola: concepción y diseño del trabajo, recolección y obtención de datos, análisis e interpretación de datos, redacción del manuscrito, y aporte de pacientes o material de estudios.
Yixi Pérez-Morales: recolección y obtención de datos, análisis e interpretación de datos, redacción del manuscrito, y aporte de pacientes o material de estudios.
Thayde Trujillo-Tirado: recolección y obtención de datos, análisis e interpretación de datos, redacción y revisión crítica del manuscrito.
Financiación
Hospital General Docente “Cptan. Roberto Rodríguez Fernández”